细胞器是细胞中不可或缺的功能单元,通常由生物膜包裹特定生物分子构成,用以维持细胞正常结构与功能。受自然界启发,科学家现已成功构建高生物相容性且具有不同功能的人工细胞器,用以调控细胞原有功能或为宿主细胞引入非天然新功能。目前人工细胞器的主要构建策略包括预制超分子组装体的细胞内吞以及胞内原位蛋白相分离凝聚,但这些方法构建的人工细胞器均面临稳定性不足的问题。针对这一关键问题,河南大学药学院抗病毒性传染病创新药物全国重点实验室的张一川团队基于前期工作中发展的细胞内非天然高分子合成方法,成功开发了一种基于生物正交点击化学的稳定多功能高分子人工细胞器胞内原位合成方法学体系,该工作以“In situ synthesis of multifunctional 3D polymeric artificial organelles in living cells”为题发表在Journal of the American Chemical Society,硕士研究生张鲁鲁为本文的第一作者,陈洁博士和张一川教授为共同通讯作者,河南大学药学院是该工作的唯一通讯单位和完成单位,该工作不仅是该课题组建立后发表的首项独立研究工作,也是河大药学院首篇独立自主产出的JACS。该工作得到国家自然科学基金、河南省教育厅重点科研项目、河南省国际科技合作项目、以及抗病毒性传染病创新药物全国重点实验室开放课题的支持。
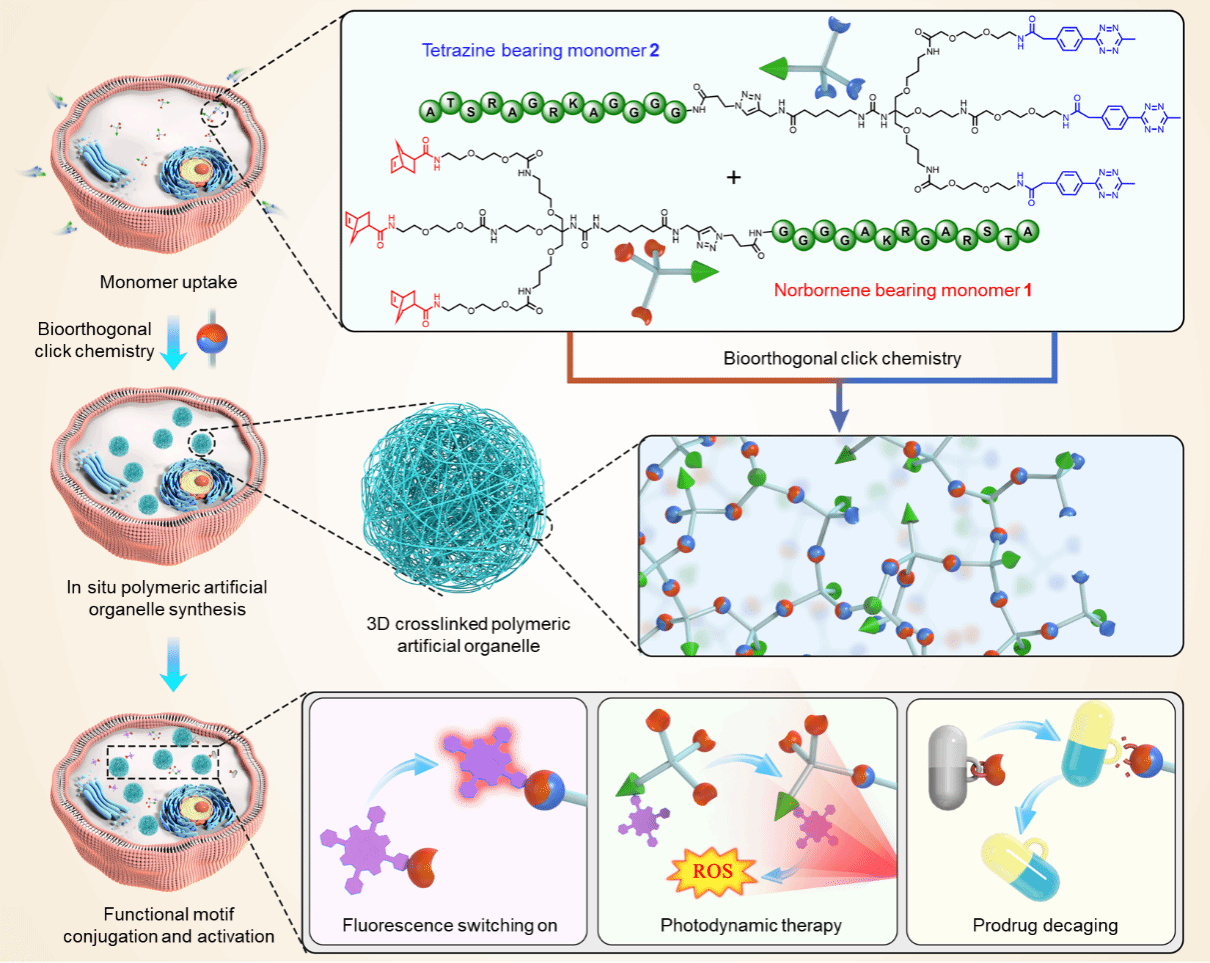
图1. 研究工作示意图
这一工作中,作者首先设计合成了含有生物正交反应活性中心和选择性细胞穿膜肽的点击聚合单体(如图1所示),并通过核磁共振氢谱、动态光散射和透射电镜对缓冲液中的聚合过程进行详细监测表征,实验结果均表明,两种点击聚合单体能够高效反应生成接近微米级的微粒,并且所合成聚合物及单体本身在生物相关环境下均具有优异的稳定性(如图2所示)。
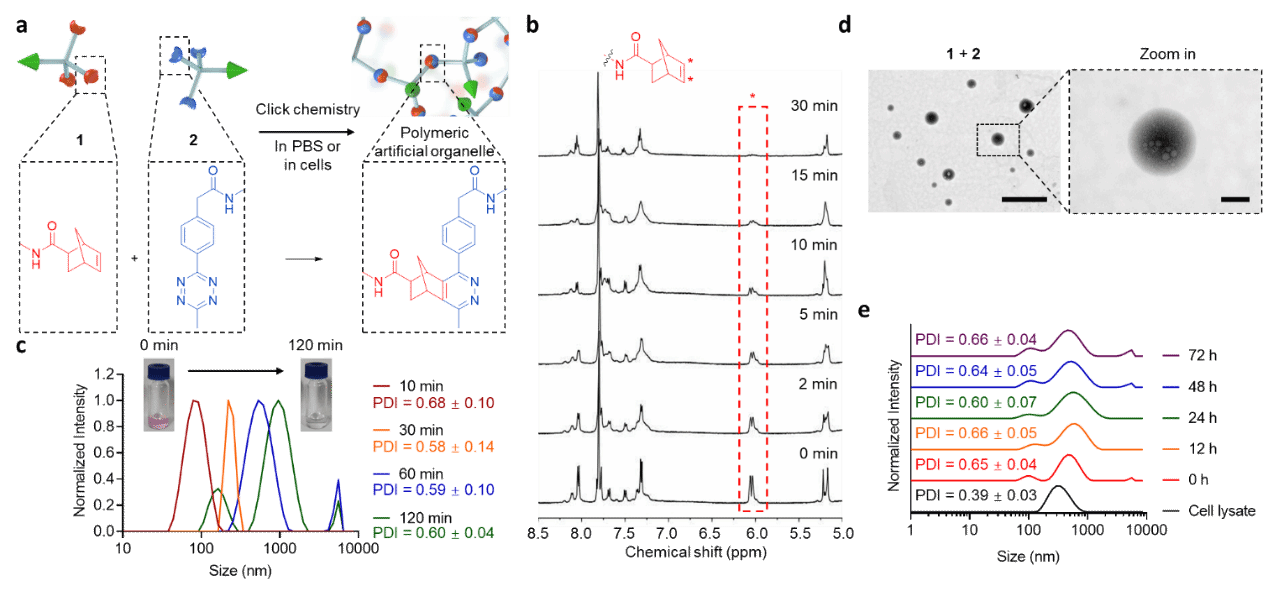
图2. 点击聚合体系的验证表征
进一步,作者对点击聚合体系的生物安全性、细胞选择性、以及胞内原位聚合效率进行了研究。如图3所示,点击聚合单体及聚合物微粒均具有良好的安全性,并且由于选择性细胞穿膜肽结构的引入,单体对p32过表达MDA-MB-231细胞系呈现优异的选择性。值得注意的是,与通过内吞方式进入细胞的传统脂质体人工细胞器不同,胞内原位合成的聚合物人工细胞器主要分布于细胞质中,仅有少量进入溶酶体,有效降低了溶酶体膜对人工细胞器与生物分子及其他功能分子相互作用的阻碍,并且降低了其被降解清除的风险。后续共聚焦显微镜等实验结果显示,两种点击聚合单体在活细胞中同样能够有效实现偶联聚合,高效生成聚合物微粒,并且其尺寸与缓冲液中所合成的微粒相当。
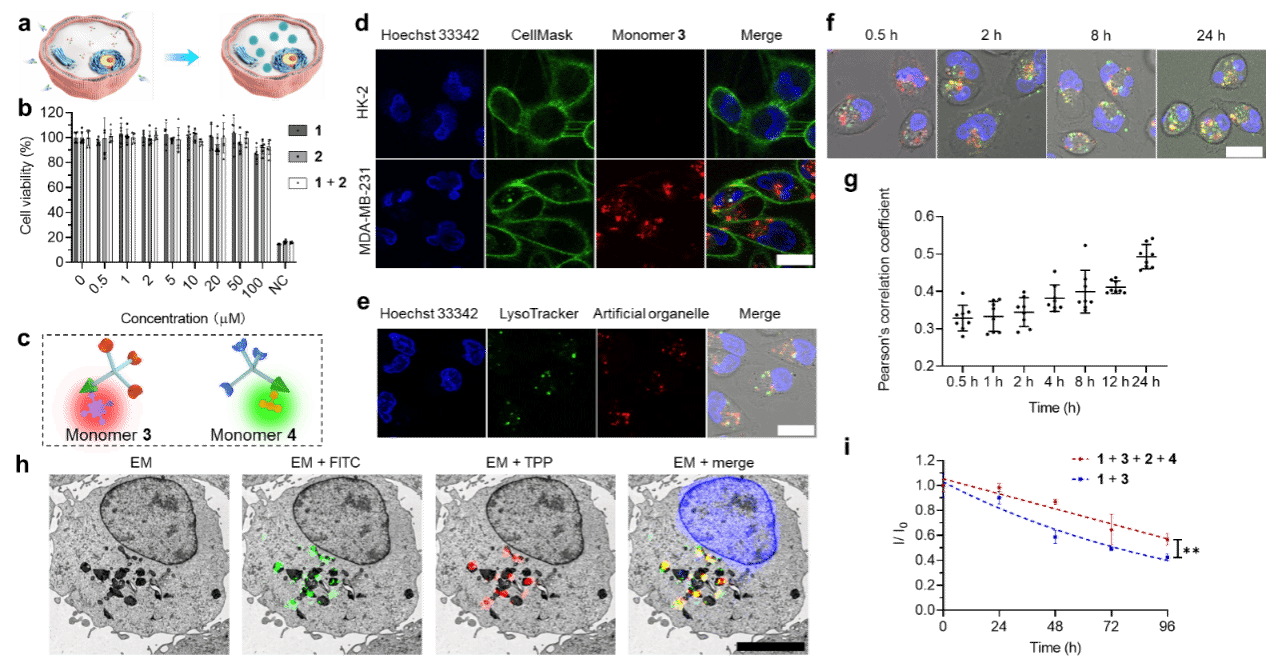
图3. 聚合物人工细胞器的胞内原位合成验证及表征
成功实现聚合物人工细胞器的胞内原位构建后,作者利用人工细胞器表面过量的四嗪反应活性中心实现了包括淬灭荧光标记分子点亮、光动力治疗光敏剂偶联、肿瘤治疗前药脱笼释放等一系列非天然功能。研究结果显示,淬灭荧光分子的引入能够实现含有人工细胞器细胞的选择性荧光标记(如图4所示);偶联光敏剂的人工细胞器在630 nm光照下可显著降低肿瘤细胞活性;笼化前药在人工细胞器表面触发四嗪-亲双烯体加成消除反应,可释放阿霉素对肿瘤细胞活性产生抑制(如图5所示)。更重要的是,作者发现负载于人工细胞器上的点击化学活性中心相比于小分子形式具有更高的稳定性和更长的胞内滞留时间,这为化学生物学相关研究及疾病诊疗方面应用提供了更多可能。
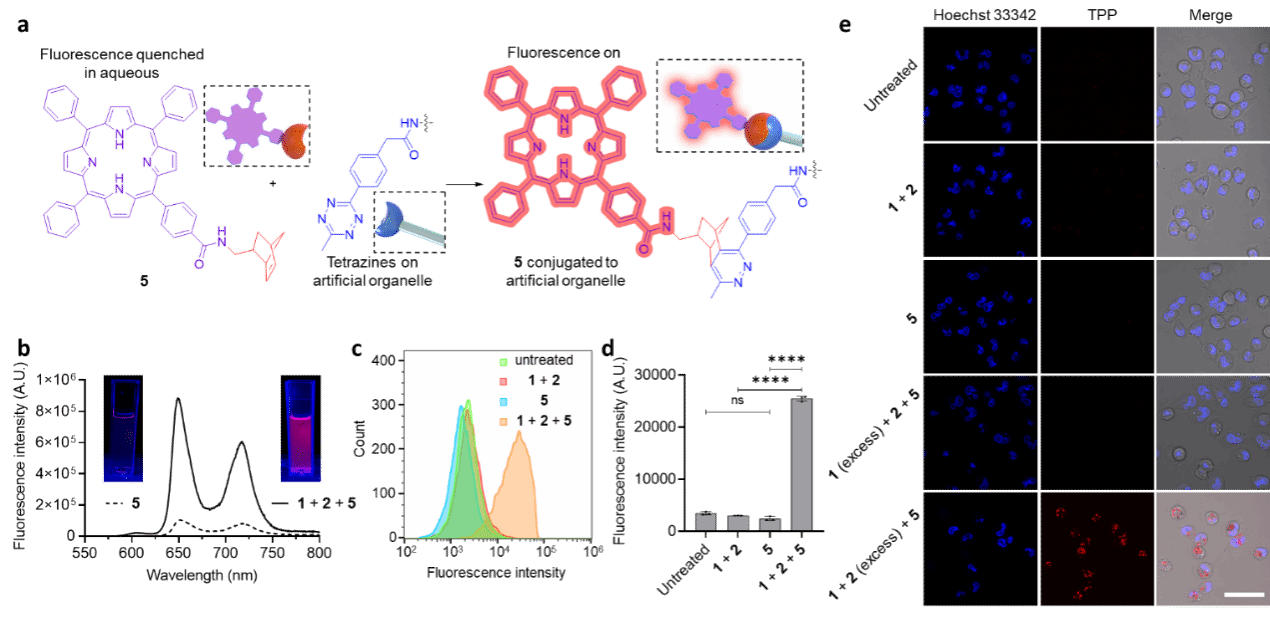
图4. 人工细胞器实现淬灭荧光标记物原为激活点亮
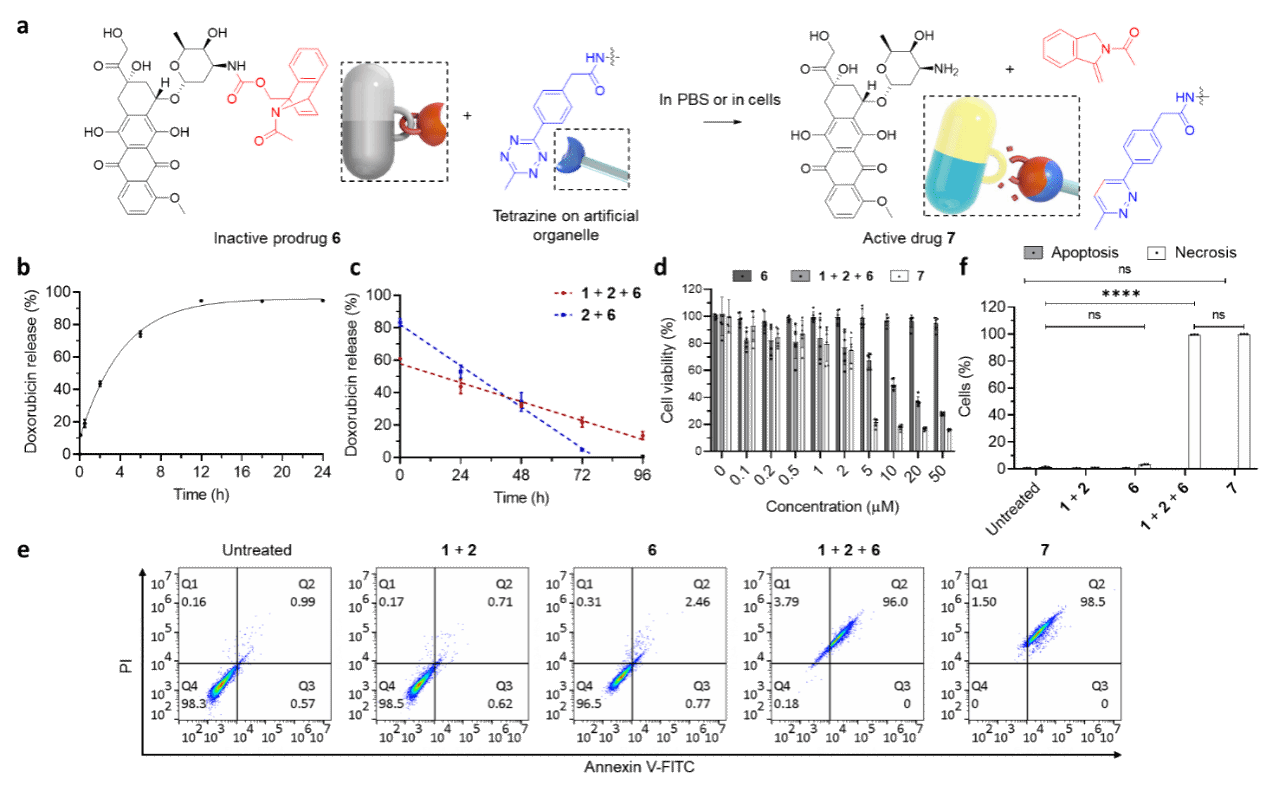
图5. 工细胞器原位实现前药脱笼激活抑制肿瘤细胞活性
综上,本研究将细胞内非天然高分子合成与人工细胞器概念有机结合,发展了一种全新的聚合物人工细胞器原位合成方法学体系,这一方法不仅为构建稳定人工细胞器提供了新途径,也为化学生物学研究提供了新的化学工具。可以预见,随着研究不断深入,相关研究工作必将有力推动人工生命体、合成生物学、活体机器人等相关领域的快速发展。

张一川课题组致力于生物正交点击化学、刺激响应小分子前药、刺激响应高分子药物递送系统·等方面研究工作,发展了多种活细胞内非天然分子结构原位构建及转化的技术方法,建立了活体内放疗X射线、可见光驱动非天然分子原位结构转化的方法学体系,并在疾病诊断治疗方面等实现了应用。
团队负责人张一川教授近年来主持国家自然科学基金项目1项,省部级项目7项,全重室开放课题1项,以第一或通讯作者在Nat. Chem.、J. Am. Chem. Soc.、JACS Au、Cell Rep. Phys. Sci.等高水平期刊发表研究论文十余篇,多项成果被C&EN、Chemistry World、Nat. Rev. Chem.等国内外主流期刊媒体引用报道,获授权国家发明专利3项,现任河南省药学会药物化学专业委员会委员。
